Resonantie hybride betekenis
Chemische resonantie [1] of mesomerie [2] is een manier om de elektronendistributie weer te geven bij bepaalde moleculen en samengestelde ionen die niet met behulp van één Lewisstructuurformule beschreven kunnen worden. Men spreekt dan over deeltjes met gedelokaliseerde elektronenparen. Een dergelijk molecuul of samengesteld ion wordt met. Resonantie (Resonantie, Opslingering, Resonance) Resonantie is de eigenschap dat bij bepaalde frequenties de afhankelijke grootheid sterk toeneemt (opslingert) bij gelijkblijvende sturende grootheid. Een ander kenmerk is dat een constructie nog even naklinkt terwijl de bron als verwijderd is. Dit naklinken kan zowel akoestisch als elektrisch. 



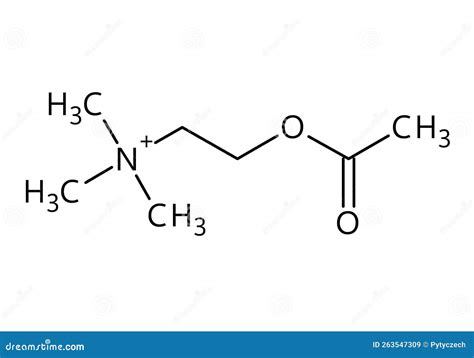
Resonantie hybride betekenis Als het maar één Lewis-structuur heeft, heeft het geen resonantie-hybride. Hoe de moleculen met resonantie te identificeren. Resonantie bestaat alleen als een Lewis-structuur meerdere bindingen heeft en een aangrenzend atoom met ten minste één alleenstaand paar. De algemene vorm van resonantie wordt hieronder geïllustreerd.
Stabiliteit molecuul
Aromaticiteit van een molecuul zegt veel over de interne potentiële energie en de stabiliteit van een molecuul. Zo zijn aromaten uiterst stabiel, hebben ze een potentiële lagere energie en reageren ze doorgaans moeilijk. Stabiliteit verwijst in de scheikunde naar een toestand van evenwicht of naar de bestendigheid van een chemisch of fysicochemisch systeem tegen interne en externe invloeden of storingsparameters. Stabiliteit is bij verschillende systemen en in verschillende chemische contexten van belang. Stabiliteit molecuul Waarom zijn molecuul stabiel? Moleculen zijn stabiel vanwege de sterke aantrekkelijke krachten tussen de atomen die ze vormen. Deze krachten zijn voornamelijk te wijten aan chemische bindingen, die het resultaat zijn van het delen of overbrengen van elektronen tussen atomen.Mesomere effect
In chemistry, the mesomeric effect (or resonance effect) is a property of substituents or functional groups in a chemical compound. It is defined as the polarity produced in the molecule by the interaction of two pi bonds or between a pi bond and lone pair of electrons present on an adjacent atom. [ 1 ]. What is Mesomeric Effect? The mesomeric effect, also known as resonance effect, refers to the induction of polarity in a molecule or a conjugated system resulting from the movement of π electrons towards or away from a substituent group. Mesomere effect Another way of shifting electron density in a molecule occurs via the resonance effect which, because of old literature, is also known as the mesomeric effect. The principal difference here is that the mesomeric effect works through π bonds.Chemische binding
Chemical bonding, any of the interactions that account for the association of atoms into molecules, ions, crystals, and other species. When atoms approach one another, their electrons interact and tend to distribute themselves in space so that the total energy is lower than it would be in any alternative arrangement. A chemical bond is an attraction between atoms. This attraction may be seen as the result of different behaviors of the outermost or valence electrons of atoms. These behaviors merge into each other seamlessly in various circumstances, so that there is no clear line to be drawn between them.- Chemische binding As Butlerov wrote, “Starting from the assumption that each chemical atom possesses only a definite and limited amount of chemical force (affinity) with which it takes part in forming a compound, I might call this chemical arrangement, or the type and manner of the mutual binding of the atoms in a compound substance, by the name of chemical.
Structuurformule
Een structuurformule is een chemische formule die de structuur en samenstelling van een molecuul of kristalstructuur weergeeft. Leer hoe je structuurformules leest, schrijft en tekenst met voorbeelden van organische, aromatische, complexe en ionische stoffen. Leer hoe je moleculen kunt tekenen en begrijpen met verschillende manieren en regels. Bekijk de video van Mark Koren, een scheikundeleraar, en oefen mee met voorbeelden en opdrachten.- Structuurformule Leer hoe je de ruimtelijke bouw van een molecuul kunt bepalen met lewisstructuren. Volg de octetregel, tekent de bindingsstreepjes en de vrije elektronenparen, en bekijk de voorbeelden en uitleg.